Presentación de Caso
Alcalosis metabólica hipoclorémica secundaria a shock séptico como forma de presentación de la Fibrosis Quística
Hypochloremic metabolic alkalosis due to septic shock as a presentation of cystic fibrosis
María Elizabeth Castillo Rodríguez 1* https://orcid.org/0009-0004-0390-6972
Rolando Santiesteban Leyva 1 https://orcid.org/0009-0008-4088-7933
Yamirka Santiesteban Castro 1 https://orcid.org/0009-0006-8044-653X
1 Universidad de Ciencias Médicas de Holguín. Facultad de Ciencias Médicas ´´Mariana Grajales Coello´´. Holguín, Cuba.
*Autor para la correspondencia. Correo electrónico: castillorodríguezm15@gmail.com
RESUMEN
La deshidratación con alcalosis metabólica hipoclorémica es una manifestación conocida de la fibrosis quística, pero infrecuente como forma de presentación. Lactante de 6 meses de edad quística que presentó alcalosis metabólica hipoclorémica con otras alteraciones hidroelectrolíticas secundaria a schock séptico de foco pulmonar. Se procedió a ingresar en Unidad de Cuidados Intensivos, acoplado inmediatamente a equipo de ventilación mecánica con apoyo de drogas vasoactivas y se planteó disfunción múltiple de órganos. Luego de un mes de estadía en el servicio se trasladó a sala de respiratorio. Se realizó estudio molecular que demostró genotipo heterocigoto para la mutación compuesta ΔF508. Existen pocos casos en la literatura de alcalosis metabólica hipoclorémica asociada a shock séptico reportados como forma de presentación de la fibrosis quística, por lo que debe considerarse su diagnóstico, sobre todo en lactantes con este tipo de depleción electrolítica y desequilibrio ácido base, incluso sin síntomas respiratorios clásicos.
Palabras clave: alcalosis, shock séptico, fibrosis quística
ABSTRACT
Dehydration with hypochloremic metabolic alkalosis is a known manifestation of cystic fibrosis, but it is uncommon as a presenting symptom. A 6-month-old infant with cystic fibrosis presented with hypochloremic metabolic alkalosis and other electrolyte disturbances secondary to septic shock of pulmonary origin. He was admitted to the Intensive Care Unit, immediately connected to mechanical ventilation equipment with vasoactive drug support, and multiple organ dysfunction was suspected. After one month in the ICU, the patient was transitioned to the Respiratory Unit. A molecular study was performed, which showed a heterozygous genotype for the compound ΔF508 mutation. There are few cases in the literature of hypochloremic metabolic alkalosis associated with septic shock reported as a form of presentation of cystic fibrosis, so its diagnosis should be considered, especially in infants with this type of electrolyte depletion and acid-base imbalance, even without classic respiratory symptoms.
Keywords: alkalosis, septic shock, cystic fibrosis
Introducción
La fibrosis quística (FQ) es una enfermedad genética autosómica recesiva, crónica, multisistémica y letal, que codifica una proteína reguladora de la conductancia transmembranal (CFTR en inglés). El CFTR normal funciona como un regulador de los canales de Na y Cl dependientes de AMP cíclico en la membrana apical de las células epiteliales, establecen un balance entre la absorción de sodio y la secreción de cloro y bicarbonato para hidratar en forma adecuada la superficie de las vías aéreas. (1)
El pediatra Guido Fanconi von Grebel utilizó por primera vez en 1936 el término «fibrosis quística» para describir la asociación de insuficiencia pancreática exocrina y enfermedad pulmonar crónica en niños. En 1945, Sydney Farber especuló que se trataba de un problema localizado no solo en el páncreas, sino una alteración generalizada en la producción de moco, por lo que acuñó el término «mucoviscidosis». Al año siguiente, Dorothy H. Andersen realizó una serie de estudios a familiares de pacientes con FQ y llegó a conclusión de que se trataba de una enfermedad genética autosómica recesiva. (2)
La misma afecta a casi 1 de cada 3000 nacidos vivos en el norte de Europa, aunque su frecuencia varía entre diferentes orígenes étnicos. Por ejemplo, para los Estados Unidos, la incidencia es de 1 por 4000 nacidos vivos, mientras que para los hispanos es de 1 por 8000-10,000. (3)
Tras analizar los datos respecto a la epidemiología, diagnóstico y manejo de la fibrosis quística en Latinoamérica, específicamente en México, Brasil, Argentina, Colombia, Chile y Ecuador, se puede observar que la incidencia en estos países es considerablemente baja al compararlo con otros con mayor presencia de población caucásica; sin embargo, este es un dato que se espera aumente con el paso del tiempo debido a una mayor investigación y capacidad de heterogenización racial. (4)
En un registro nacional realizado en 2019 se demostró que la prevalencia de fibrosis quística en Cuba es de 26,3 casos por 1.000.000 de habitantes. La edad media en el momento del diagnóstico es de 2 años y la edad media de la población total es de 15 años. De los mayores de 16 años, la prevalencia de infección por Pseudomonas aeruginosa lo conformó el 46 %, el 36 % lo constituyó la prevalencia de infección por Staphylococcus aureus y el 80 % de los individuos recibían azitromicina oral. La mutación genética más común fue F508 observada en el 50 % de los pacientes. (5)
En la provincia Holguín son siguidos en consulta multidisciplinaria 22 casos de fibrosis quística de los cuales el 30,6 % supera los 15 años. (6)
Esta enfermedad se puede presentar con una amplia variedad de síntomas y signos, los cuales varían desde el período de recién nacido a la adultez. Su presentación clínica característica, más allá de la etapa neonatal, puede ser por manifestaciones respiratorias, digestivas, afectación hepática y pancreatobiliar, nasosinusal y anomalías urogenitales en pacientes de sexo masculino. (7)
La deshidratación con alcalosis metabólica hipoclorémica es una manifestación conocida de la fibrosis quística, pero infrecuente como forma de presentación. (7) El objetivo de este informe es presentar el caso de un lactante de 6 meses de edad cuya forma de debut de la fibrosis quística fue la alcalosis metabólica hipoclorémica secundaria a schock séptico de foco pulmonar.
Presentación del Caso
Motivo de ingreso: dificultad para respirar.
HEA: Lactante masculino de 6 meses de edad, raza mestiza, procedencia rural, con antecedentes patológicos personales de reflujo gastroesofágico con seguimiento por Pediatría y Gastroenterología. No presentaba antecedentes patológicos familiares ni antecedentes prenatales, perinatales ni posnatales de importancia.
Sus padres lo trasladan al Hospital Pediátrico ¨Octavio de la Concepción y la Pedraja¨y es recibido en el Cuerpo de Guardia, ya que presentaba disnea de intensidad variable desde hacía 3 días que cedía con la administración de aerosol de Salbutamol, acompañada de tos productiva, así como rechazo de los alimentos excepto el pecho, vómitos; dificultad respiratoria que se intensificó y se acompañó de somnolencia mantenida. Además, refiere la madre la presencia de heces fétidas y esteatorreicas. Por todo lo anterior se decidió su ingreso para estudio y tratamiento.
Al ingreso presentó un peso de 5500 gramos y talla 63 cm por lo que de acuerdo a la valoración nutricional el peso para la edad, la talla para la edad y el peso en correspondencia con la talla estaban por debajo del tercer percentil.
Al examen físico se evidenciaron mucosas secas e hipocoloreadas, polipnea, tiraje intercostal, frecuencia respiratoria 52 respiraciones/ minuto. Se auscultaron estertores crepitantes en base pulmonar derecha. Al examen del sistema cardiovascular se constató frecuencia cardíaca de 164 latidos/minuto, pulsos distales débiles, llene capilar enlentecido 25 y gradiente térmico y manifestaciones neurológicas de hipotonía muscular y apatía, así como fontanela anterior deprimida.
La conducta diagnóstica incluyó hemograma completo con eritrosedimentación, la cual mostró una hemoglobina en 67 g/L, traducida en una anemia severa. El estudio de lámina periférica reveló anisocromía, anisocitosis, microcitosis y leucocitos normales con ligera linfocitosis. Además, se realizó radiografía de tórax en vista posteroanterior donde se observaron engrosamientos perihiliares bilaterales y aumento de la radiopacidad en la región paracardíaca derecha. (Ver figura 1).
El ionograma y la gasometría mostraron valores de ph de 7,548; la PO2 143,5 mmHg; K+ 1,82 mmol/L; Cl- 92,3 mmol/L; [HCO3] 31,7 mmol/L; EB 8,7 mmol/L compatible con Alcalosis Metabólica Hipoclorémica con Hipopotasemia. En la tabla I se muestran los valores de hemogasometría e ionogramas seriados que evidencian la evolución del paciente en los días posteriores al ingreso. (Ver tabla I).
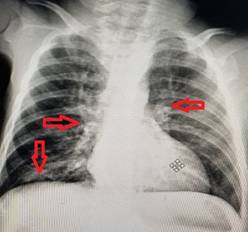
Fig. 1. Radiografía de Tórax vista PA
Tabla I. Evolución temporal de los valores seriados de hemogasometría e ionograma del paciente con debut de fibrosis quística.
|
Parámetros |
24/9/24 |
26/9/24 |
28/9/24 |
30/9/24 |
2/10/24 |
3/10/2024 |
|
Lonograma |
|
|||||
|
Na+ (mmol/L) |
146,8 |
135,3 |
141,2 |
139,9 |
140,3 |
140,0 |
|
K+ (mmol/L) |
1,82 |
5,31 |
5,66 |
2,30 |
2,68 |
4,46 |
|
Cl- (mmol/L) |
99,6 |
92,3 |
96,8 |
96,6 |
96,6 |
99,9 |
|
Ca2+ (mmol/L) |
1,099 |
1,044 |
0,845 |
0,931 |
1,053 |
1,077 |
|
Gasometría |
|
|||||
|
Ph |
7,548 |
7,471 |
7,470 |
7,602 |
7,472 |
7,494 |
|
PCO2 (mmHg) |
37,2 |
51,6 |
45,6 |
29,9 |
43,6 |
37,0 |
|
pO2 (mmHg) |
143,5 |
152,9 |
185,1 |
No calibrado |
109,7 |
65,1 |
|
HCO3 (mmol/L) |
31,7 |
36,8 |
32,4 |
28,8 |
31,1 |
27,8 |
|
EB (mmol/L) |
8,7 |
11,9 |
7,8 |
7,4 |
6,8 |
4,3 |
Fuente: Historia Clínica Individual
Se ingresó en Unidad de Terapia Intensiva Pediátrica, reportado de crítico con alto riesgo para la vida, inmediatamente acoplado al equipo de ventilación mecánica, con apoyo de drogas vasoactivas (dobutamina 250 mcg/10 ml a dosis de 10mcg/kg/min en infusión IV), sedación con midazolam.
Se le aspiraron secreciones purulentas por el tubo endotraqueal, por el abordaje venoso periférico femoral se le indicó hidratación rápida y posteriormente de mantenimiento, y se realizó la corrección del desequilibrio hidroelectrolítico.
Se planteó el síndrome de disfunción múltiple de órganos por compromiso de los sistemas digestivo, respiratorio, cardiovascular y neurológico. Se impuso tratamiento antimicrobiano empírico con ceftriaxona.
Seguidamente se realizó hemocultivo en pico febril donde resultó aislado Acinetobacter iwoffi, cepa productora de carbapenemasa (metalobetalactamasa) resistente a penicilinas, cefalosporinas y carbapenémicos (meropenén) y candida spp. Se realizó CIM de colistina ≤ 2mg/mc a la cual se mostró sensible.
Se sustituyó el tratamiento anterior por meropenen (bulbo 50mg/10ml a dosis de 60mg/kg/día) asociado a colistina (100mg/2ml a dosis de 5mg/kg/día), aparte de anfotericin B (bulbo de 50 mg/10ml a dosis de 0,50mg/kg/día). Después de una estadía de un mes en el servicio se trasladó a sala de respiratorio en aislamiento.
El paciente fue valorado por el servicio de Genética, en la que se indicó estudio molecular, el cual demostró que el paciente era heterocigoto compuesto genotípicamente para la mutación ΔF508 de la Fibrosis Quística y por tanto enfermo fenotípicamente. Se brindó asesoramiento genético a los padres y se indicó posteriormente estudio molecular al hermano y padres del lactante. En espera de realizar prueba de Electrólitos del Sudor.
Discusión
Este caso ilustra una forma de presentación atípica de la Fibrosis Quística caracterizada por alcalosis metabólica hipoclorémica con hipopotasemia.
Según Ampuero et.al, muchos de los factores asociados a este tipo de depleción electrolítica y desequilibrio del medio interno en el paciente con Fibrosis Quística se encuentran presentes: una edad menor de un año, existencia de deshidratación, exposición reciente a temperatura ambiental elevada, incremento de la temperatura corporal e infección respiratoria intercurrente, alimentación materna exclusiva o con fórmulas con bajo contenido de sodio insuficiente en lactantes. (7)
En la fisiopatología de esta afección se destaca que en los pacientes con FQ la producción primaria de sudor es relativamente normal; sin embargo, la existencia de una deficiente absorción de cloro origina una falla en la activación de los canales de sodio y ante escenarios que originen una sudoración excesiva, se excreta una gran cantidad de NaCl y por consiguiente pérdida de estos electrolitos como también de fluidos por esta vía. (7)
Esto causa activación del sistema simpático, incremento en la liberación de la hormona antidiurética y activación del eje renina- angiotensina-aldosterona con desarrollo de hiperaldosteronismo secundario, lo que ocasiona reabsorción de sodio y agua y excreción de potasio e hidrogeniones en el túbulo colector cortical renal; además la depleción de cloro origina alcalosis metabólica por reabsorción renal de bicarbonato, lo cual recibe en la actualidad el nombre de alcalosis metabólica por depleción de cloro y permite destacar así el rol trascendental de la falta del cloro en su origen. (7)
Los autores concuerdan con el papel del schock séptico como desencadenante de deshidratación aguda y empeoramiento de las alteraciones electrolíticas, en el que se encontraron similitudes con este caso: una lactante de 3 meses con infección mixta por Rhino/enterovirus y S. pneumoniae asociada a schock séptico. El mismo resalta la importancia de sospechar FQ incluso sin síntomas pulmonares clásicos, especialmente en países sin tamizaje neonatal. (7)
La falla en el medro y los trastornos hidroelectrolíticos de los lactantes se presentan por múltiples causas, pero la deshidratación hipoclorémica con alcalosis metabólica es infrecuente y se ha descrito principalmente en los casos de vómito recurrente por un síndrome pilórico, vómito persistente de diversa etiología, drenaje del contenido gástrico (por sondas gástricas) con inadecuado reemplazo de las pérdidas, ingesta de álcalis en estados asociados a hipokalemia (hiperaldosteronismo), pérdida excesiva de cloro por la piel en la FQ o por síndrome de Bartter. (7,8,9)
En los casos de dos lactantes con clínica de alcalosis metabólica con hipocloremia presentados por Morales et al., se tuvo en cuenta que no hubo ninguna pérdida gastrointestinal observable pues los pacientes no tenían vómitos incoercibles, ni diarreas de gasto elevado, ni sondas gástricas y la opción restante era la pérdida por la piel, con un comportamiento semejante al paciente presentado. (8)
Otro de los diagnósticos diferenciales a considerar en el paciente por la presencia de vómitos ante la ingestión de alimentos fue la estenosis hipertrófica del píloro, donde se produce alcalosis por la pérdida de hidrogeniones por vómitos sin embargo en esta patología no se presenta hipokalemia ni hiponatremia. (7,10)
El síndrome de Bartter obedece a una alteración congénita en la reabsorción tubular de cloro (mutación de la proteína del canal iónico de cloro-Kb), por lo que a diferencia del paciente con FQ aquí las pérdidas de cloro son de origen renal. Este se caracteriza por presentar además de las alteraciones de laboratorio previamente mencionadas, hipokalemia grave e hiperreninemia. (7,10)
Otras condiciones más infrecuentes de observar y las cuales son catalogadas como síndrome de pseudo-Bartter, dada la similitud bioquímica, son la diarrea perdedora de cloruros, las pérdidas gástricas continuas sin una adecuada reposición y el uso excesivo o mal uso de diuréticos de asa. (7,10)
En un estudio retrospectivo realizado de enero de 2015 a diciembre de 2019 en el Hospital Universitario Aga Khan (AKUH), Pakistán, solo 6 de los 72 pacientes pediátricos ingresados presentaron características consistentes con Síndrome de PseudoBartter, que llevaron al diagnóstico de fibrosis quística etiquetados como "presentadores tempranos".(10) Esto concuerda con los resultados expuestos ,ya que resalta que se trata de una forma atípica de presentación que debe evaluarse ante un lactante con este cuadro clínico.
Además, se encontró que en este grupo la colonización por Pseudomonas fue menos frecuente, (10) como es el caso del resultado de hemocultivo en pico febril que se realizó de este lactante, en el cual se encontró una colonización mixta por Acinetobacter y Chlamidia. Este hecho resulta de vital importancia, ya que constituye otro rasgo atípico que puede desorientar el diagnóstico.
En comparación con un caso de México publicado en 2016, donde se describe un lactante con tos crónica como parte del fenotipo sinopulmonar crónico, alcalosis metabólica crónica, fenotipo perdedor de sal y desnutrición como parte del síndrome nutricional-gastrointestinal, (11) en el caso mostrado el paciente solo presentaba antecedentes patológicos personales de Reflujo Gastroesofágico y en la clínica una falla de medro asociada a heces fétidas y esteatorreicas.
Se han descrito varias mutaciones del gen CFTR asociadas con deshidratación, hiponatremia y alcalosis metabólica, tales como F311L, D110E, D110H, T3381, N1303K, 2,789 + 5G-A, S13F y 3849 + 40 A/G 9 10 11 12 13 14 15 16. El paciente descrito en este artículo se presentó con mutación DF508 que, aunque es una de las mutaciones más frecuentes asociadas a FQ, no ha sido reportada frecuentemente con SPB, ya que habitualmente produce el cuadro clínico típico de forma temprana, con lo cual el diagnóstico se hace con antelación. (11)
En cuanto al diagnóstico, Desvaux García y colaboradores han planteado que la introducción de TIR (tripsina inmunorreactiva) dentro de los estudios del cribado neonatal, ha supuesto una disminución de los ingresos hospitalarios de los pacientes con FQ debido a que se pueden anticipar las posibles complicaciones cuando se lleva a cabo un proceso eficiente de comunicación con las familias; a propósito de un lactante de ocho meses con deshidratación hiponatrémica, en el año 2019, con 12 horas de evolución, secundario a vómito y disminución de la ingesta e hipocloremia grave. (12)
Conclusiones
Este caso subraya la importancia de considerar la fibrosis quística (FQ) como diagnóstico diferencial en lactantes que presentan alcalosis metabólica hipoclorémica con hipopotasemia severa, incluso en ausencia de síntomas respiratorios clásicos. La presentación atípica, desencadenada por un shock séptico pulmonar, resalta cómo una infección intercurrente puede precipitar y enmascarar una deshidratación electrolítica crónica propia de la FQ. Resulta novedoso el hallazgo de una colonización mixta por Acinetobacter y Candida en lugar de los patógenos típicos, lo cual podría retrasar la sospecha clínica. El genotipo heterocigoto compuesto ΔF508, aunque frecuente, no suele asociarse comúnmente al síndrome de pseudo-Bartter como forma de debut.
Referencias Bibliográficas
1. González Torres A. Características clínicas, espirométricas, radiográficas y farmacológicas de pacientes con fibrosis quística atendidos en la clínica de cuidados paliativos en un hospital de tercer nivel[Tesis].[México]:Universidad Nacional Autónoma de México;2024. 55p. Disponible en: https://ru.dgb.unam.mx/bitstream/20.500.14330/TES01000854498/3/0854498.pdf
2. Redondo Sancho R, Sancho Almau R, Prades Laborda E, Lathapia Callen M, Sancho Almau J, Pérez Tella N. Fibrosis quística: artículo monográfico. 2024[citado 02/06/2025];5(8). Disponible en: https://revistasanitariadeinvestigacion.com/fibrosis-quistica-articulo-monografico-2/
3. Vargas Roldán SY, Lezana Fernández JL, Cerna Cortés JF, Partida Sánchez S, Santos Preciado JI, Rosales Reyes R. Fibrosis quística: patogenia bacteriana y moduladores del CFTR (regulador de conductancia transmembranal de la fibrosis quística). Bol Med Hosp Infant Mex.2022 [citado 23/08/2025];79(4): 215-221.Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1665-11462022000400215&lng=es
4. Corcho Forero M. Perspectivas regionales de la fibrosis quística: epidemiología, diagnóstico y manejo en países de América Latina[Tesis].[Colombia]:Universidad de los Andes; 2024.26p. Disponible en: https://repositorio.uniandes.edu.co/entities/publication/21cb2cf8-19be-46f4-aa24-7b0626b26a7b
5. Rodríguez Calá F, Suárez Medina R, Venero Fernández SJ, Smyth A, Carr SB, Fogarty AW. The prevalence, clinical status and genotype of cystic fibrosis patients living in Cuba using national registry data. J Cyst Fibros. 2019[citado 06/08/2025];18(4):522-524.Disponible en: https://www.cysticfibrosisjournal.com/article/S1569-1993(18)30859-2/fulltext
6. Peña Ramírez D, Medrano Santos E, Taño Tamayo D. Aspectos microbiológicos de las infecciones respiratorias en pacientes con fibrosis quística en el Hospital Pediátrico de Holguín, octubre 2021-junio 2022[Tesis].Holguin, Cuba]: Universidad de Ciencias Médicas Holguín; 2023.18p.Disponible en: https://cisalud-ucmh.sld.cu/index.php/cisalud/2023/paper/viewFile/598/244
7. Ampuero Acuña C, Tomarelli Rubio G, Montes Franceschini S, Donoso Fuentes A. Depleción electrolítica extrema asociada con shock séptico como forma de presentación de fibrosis quística. Andes pediatr. 2022 [citado 23/08/2025];93(1):110-116. Disponible en: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S2452-60532022000100110&lng=es
8. Morales Múnera OL, Villada Valencia JC, Flórez ID, Pineda Trujillo NG. Alcalosis metabólica hipoclorémica como presentación de la fibrosis quística. Informe de dos casos. Iatreia.2013 [citado 23/08/2025]; 26(3):356-365.Disponible en: http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0121-07932013000300011&lng=en.
9. Galaviz Ballesteros MJ, Acosta Rodríguez Bueno CP, Consuelo Sánchez A, Franco Álvarez I, Olalla Mora OI, Vázquez Frias R. Síndrome de pseudo-Bartter como presentación de fibrosis quística con mutación DF508. Bol Med Hosp Infant Mex. 2016 [citado 06/07/2025];73(5): 331-334. Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1665-11462016000500331&lng=es.
10. Ballestero Y, Hernandez MI, Rojo P, Manzanares J, Nebreda V, Carbajosa H, et al. Hyponatremic Dehydration as a Presentation of Cystic Fibrosis. Pediatr Emerg Care. 2006[citado 06/07/2025];22(11):725-727.Disponible en: https://journals.lww.com/pec-online/abstract/2006/11000/hyponatremic_dehydration_as_a_presentation_of.8.aspx
11.Abdul Aziz D, Siddiqui F, Abbasi Q, Iftikhar H, Shahid S,Mir F. Characteristics of electrolyte imbalance and pseudo-bartter syndrome in hospitalized cystic fibrosis children and adolescents, J Cyst Fibros.2022[citado 06/08/2025];21(3):514-518. Disponible en: https://www.sciencedirect.com/science/article/pii/S1569199321014181
12. Desvaux García M, Martín de VC, García Romero R. Tripsina inmunorreactiva para la detección de pacientes con fibrosis quística. Rev Mex Pediatr. 2023[citado 06/08/2025];90(4): 153-155. Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0035-00522023000400153&lng=es.
Conflicto de intereses
Los autores declaran que no existen conflictos de
intereses
Financiación
Los autores no recibieron financiación para el
desarrollo del presente artículo.
Declaración de autoría
MECR: conceptualización, recursos, supervisión, administración del proyecto,
diseño de la metodología, redacción-borrador original, investigación.
RSL: investigación, redacción-borrador original, análisis formal, visualización
y edición.
YSC: investigación, recursos, redacción-borrador original, análisis formal,
asesoramiento metodológico.
|
Publicación cuatrimestral de la Universidad de Ciencias Médicas de Holguín |
|
|
|
CC-BY-NC 4.0 |