HolCien 2020; 1(3)
ISSN: 2708-552X RNPS: 2495
Artículo de Revisión
Uso clínico de los marcadores tumorales en las neoplasias malignas
Clinical use of tumor markers in malignant neoplasms
Est. Belén de la Caridad Santiesteban Rodríguez1* http://orcid.org/0000-0002-4616-7020
Est. Raúl Javier Pizarro Hechavarría1 http://orcid.org/0000-0003-3586-3968
1Facultad de Ciencias Médicas Mariana Grajales Coello. Universidad de Ciencias Médicas de
Holguín, Cuba.
*Autor para la correspondencia. Correo electrónico: belensantiesteban4@gmail.com
Recibido: 12/05/2020.
Aprobado: 10/09/2020.
RESUMEN
Los marcadores tumorales son moléculas que pueden estar elevadas en presencia de un proceso neoplásico, bien como reacción del huésped o producto del propio tumor. Estos marcadores, cuya concentración sérica también depende de la variabilidad biológica del paciente, son detectables en diferentes fluidos biológicos. Se realizó una revisión de 27 referencias bibliográficas con el objetivo de describir el uso clínico de los marcadores tumorales en el cáncer donde se consultaron fuentes de información de las Ciencias Médicas. La concentración del marcador refleja el éxito de un procedimiento terapéutico tal como la cirugía, la quimioterapia. Se concluyó que un aumento del valor de los marcadores tumorales no siempre sugiere la presencia de cáncer; su principal uso es en el pronóstico y seguimiento.
Palabras Claves: Marcador tumoral; Cáncer; Pronóstico.
ABSTRACT
Tumor markers are molecules, which can be elevated in the presence of a neoplastic process, either as a host reaction or as a consequence of the tumor itself. These molecules, whose serum concentration also depends on the biological variability of the patient, are detectable in different biological fluids. A review of 27 bibliographic references was carried out in order to describe the updated clinical use of tumor markers in cancer, where sources of information from Medical Sciences were consulted. The concentration of the marker reflects the success of a therapeutic procedure such as surgery, chemotherapy. It was concluded that an increase in the value of tumor markers does not always suggest the presence of cancer; its main use is for prognosis and monitoring.
Key Words: Tumor marker; Cancer; Prognosis
Introducción
Se define como marcador tumoral a una amplia variedad de sustancias biológicas producidas o inducidas por las células tumorales o por el organismo en respuesta a su presencia, que refleja su crecimiento y pueden hallarse en sangre, orina, líquido o pleural, la mayor parte de ellos son proteínas. (1)
Estos no son nuevos en la práctica médica, su historia se remonta a mediados del siglo XIX, cuando Henry Bence-Jones informó la precipitación de una proteína en la orina acidifiada de un paciente con mieloma múltiple, el primer marcador tumoral, que se conoce como proteína de Bence-Jones, aún vigente en la práctica. (2)
Entre 1928 y 1963 los científicos describieron numerosas hormonas y su producción ectópica entre ellas la gonadotropina coriónica, enzimas, como la fosfatasa alcalina y otras proteínas que alteran sus concentraciones sanguíneas en presencia de enfermedades malignas. (2)
A finales de la década del 30 del siglo pasado la fosfatasa ácida que fue el primer marcador tumoral para el cáncer de próstata y fue utilizada hasta 1990, cuando fue reemplazada por el antígeno prostático específico descubierto en 1979 por Wang y colaboradores. (2)
En 1963 se descubrió la alfafetoproteína como marcador del hepatocarcinoma y en 1965 el antígeno carcinoembrionario como marcador de las neoplasias colorrectales, aún continúan vigentes en la práctica médica. (2)
Fueron Premios Nobel por el descubrimiento del radioinmunoanálisis: Berson y Yalowen 1958, Köhler y Milstein por el descubrimiento de los anticuerpos monoclonales en 1975, quienes, sin duda alguna, con la introducción de esta metodología abrieron el espacio para otros marcadores tumorales como el antígeno de cáncer 125 (CA 125), el 15-3 (CA 15-3) y el 19-9 (CA 19-9) para el cáncer de ovario, de mama y el digestivo, respectivamente. (2)
En la actualidad estos son muy empleados, en una auditoría realizada en Irlanda del Norte, encontró que, aunque el 80 % de las solicitudes de marcadores tumorales se relacionaban con el órgano implicado, un 54 % de los clínicos utilizaban estos como cribado de patologías malignas, con un bajo índice de sospecha en el 35 % de los casos. (3)
Otra auditoría en un hospital de Inglaterra se encontró que el 26 % de todas las solicitudes del marcador 15.3 del cáncer de mama fueron para varones, pacientes a los que en ningún caso se les había practicado biopsias en el año del estudio ni en los dos años previos. (3)
Lo mismo ocurrió en el marcador CA 125 del cáncer de ovario, que fue solicitado en un 17 % a varones. En un estudio griego, solo un 20 % de los 10 291 resultados revisados de forma retrospectiva, en 1 944 resultaron ser en pacientes con cáncer. El nivel más bajo de determinaciones apropiadas fue para el CA 19.9, 1,9 % y un 26 % de peticiones de CA 125 fueron solicitadas a varones. El marcador CEA de tumor colorrectal fue más frecuentemente solicitado de forma correcta, 27 %.(3)
Los avances en tecnologías, como la genómica, oncoproteómica, bioinformática y nanotecnología, están facilitando el descubrimiento de numerosos marcadores tumorales y están ayudando a generar hipótesis que deberán ser probadas de manera prospectiva en la clínica. (3)
El problema del cáncer es uno de los desafíos más relevantes de nuestra época. Como consecuencia de la transición demográfico-epidemiológica, este es actualmente una de las principales causas de muerte en el mundo.
El problema del cáncer está cambiando en su escala y perfil. Se estima que el número de casos nuevos anuales pasará de alrededor de 14 millones en 2017 a más de 20 millones en 2030, y que casi dos tercios de esos ocurrirán en los países menos desarrollados. En tanto que estos últimos no cuentan con recursos similares a aquellos de los países desarrollados para enfrentar la enfermedad, esta situación plantea un desafío dramático para gobiernos y autoridades sanitarias.(4)
En Cuba, los tumores malignos constituyen la segunda causa de mortalidad desde el año 1958, según datos del Anuario Estadístico se diagnostican más de 33 000 casos nuevos cada año. Al cierre del 2019 murieron 21 316 personas, lo que representó 17,9 años de vida potencialmente perdidos, siendo la primera causa de muerte en ocho provincias del país: La Habana, Villa Clara, Sancti Spíritus, Cienfuegos, Las Tunas, Granma, Santiago de Cuba, Guantánamo, y el municipio especial Isla de la Juventud.(5)
Debido a la prevalencia del cáncer a nivel mundial y al número de muertos que este ocasiona es necesario el empleo de todas las herramientas para un diagnóstico precoz, un tratamiento oportuno y así lograr un pronóstico favorable. Por esto nos planteamos la realización de esta investigación con el objetivo de describir el uso clínico de los marcadores tumorales en el cáncer ya que tienen un valor considerable en el seguimiento de los pacientes oncológicos, así como en la detección de las recidivas del cáncer incluso antes de que aparezcan sus manifestaciones clínicas.
Desarrollo
Clasificación
Los marcadores tumorales pueden agruparse según dos criterios: uno basado en el origen y otro basado en su utilidad clínica, según su sensibilidad y especificidad.
Con base en su origen, se han clasificado en dos grupos: los producidos por las células tumorales, que se denominan “derivados del tumor”; y los inducidos por la presencia del mismo y producidos por el huésped, que se llaman “asociados al tumor”. (6)
Entre los primeros estarían la mayoría de los marcadores tumorales más conocidos: antígeno carcinoembrionario (CEA), alfafetoproteína (AFP), antígeno prostático específico (PSA), la subunidad beta de la hormona gonadotropina coriónica humana (beta HCG). Entre los
segundos se incluyen proteínas de fase aguda (PCR, ferritina) y moduladores del sistema inmune (citocinas o interleucinas). (7)
La sensibilidad se define como el porcentaje de pacientes portadores de un determinado tumor, con valores patológicos, superiores a la normalidad, de un determinado marcador (su opuesto serían los falsos negativos). Se considera especificidad el porcentaje de pacientes sin un tumor maligno, con valores normales de un determinado marcador (su opuesto serían los falsos positivos). (7)
Tabla I: Valores de referencia de los marcadores tumorales y las causas no neoplásicas de su elevación.
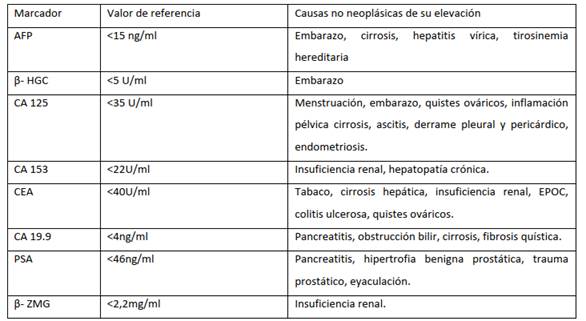
*Carvajal Garcés CF. Sensibilidad y especificidad de los marcadores tumorales. Rev. méd. Cochabamba. [Internet]. 2010
De este modo, basándose en su utilidad clínica, el marcador tumoral ideal sería aquél que solo pudiera detectarse en pacientes con cáncer (especificidad 100 %) y que además esta detección pudiera llevarse a cabo en los estadios más precoces de la enfermedad (sensibilidad 100 %). Es obvio que este marcador tumoral ideal no existe por el momento. (7)
De acuerdo con estos criterios de sensibilidad y especificidad, los marcadores tumorales podrían clasificarse en tres grandes grupos:
- Marcadores tumorales de muy elevada especificidad y sensibilidad. (7)
En el primer grupo se incluyen los marcadores tumorales que pueden ser detectados en diversas situaciones fisiológicas, en ausencia de éstas o, ante incrementos importantes, indican casi siempre la presencia de un tumor maligno. Los máximos exponentes de este grupo son la beta-HCG y la calcitonina.
- Marcadores tumorales de especificidad y sensibilidad variable. (7)
En el segundo grupo se incluyen los marcadores tumorales con sensibilidad y especificidad bajas en los estadios iniciales, con valores séricos indistinguibles en la mayoría de los casos de los hallados en sujetos sanos o en pacientes con algunas enfermedades benignas. Por el contrario, en los estadios avanzados, las concentraciones séricas de estos marcadores permiten asegurar que se trata de un tumor maligno. (1)
En este grupo se incluyen la mayoría de los marcadores tumorales utilizados en la práctica clínica: PSA, AFP, CEA, el antígeno carbohidratado 125 (CA 125), el antígeno carbohidratado 153 (CA 15.3), la enolasa neuronal específica (NSE) y el antígeno carcinoma de células escamosas (SCC). (7)
- Marcadores tumorales de baja especificidad. (7)
En el tercer grupo, esto es, el de los marcadores tumorales de baja especificidad se incluye los marcadores tumorales con una sensibilidad dependiente del estadio, pero cuya especificidad es baja, incluso en fases avanzadas de la enfermedad. Se incluyen enzimas como la lactato deshidrogenasa (LDH) o antígenos asociados a citoqueratinas, como la citoqueratina 19 (CYFRA 21). (7)
Ante la detección de un valor elevado de cualquier marcador, es necesario discriminar si dicha elevación es debida o no a la presencia de un tumor.
Para ello se utilizan tres criterios
- Concentración sérica del marcador. Por regla general, las concentraciones séricas de la mayoría de los marcadores que se pueden observar en ausencia de neoplasia suelen ser moderadas, y en cualquier caso muy inferior a las que se detectan en pacientes con metástasis. (8)
Cuanto mayor es la concentración de un marcador tumoral detectado en un paciente, mayor es la probabilidad de que se trate de un tumor maligno; por ejemplo, valores superiores a 40 ng/ml para la NSE, a 20 ng/ml para el CEA o por encima de 500 U/ml para el CA 125 o el antígeno carbohidratado 199 (CA 19.9). (8)
- Descartar patología benigna. Las hepatopatías crónicas y la insuficiencia renal son las dos principales causas de falsos incrementos (en general moderados), de los marcadores tumorales. Además, hay determinados marcadores tumorales que pueden tener una fuente especial de falsos positivos, como ocurre con el SCC y las enfermedades dermatológicas, el CA 19.9, la colestasis y el CA 125 en la existencia de derrames. (8)
- Control evolutivo. El hallazgo de concentraciones elevadas de cualquier marcador, de forma aislada, tiene un valor limitado. Es necesario realizar dos o tres determinaciones seriadas con un intervalo superior a la semivida plasmática del marcador (tiempo que tarda una sustancia en descender su concentración a la mitad) y estudiar estos resultados en conjunto. (8)
En general debe transcurrir un plazo mínimo de 15 días entre determinaciones y los incrementos o decrecimientos han de superar el 20 % para ser significativos. Si las cifras del marcador sufren un incremento continuo, se puede afirmar con bastante seguridad que el origen es tumoral. Por el contrario, si los valores no se modifican o incluso tienden a descender, habrá que buscar el origen en otra patología. (8)
Desventajas de los marcadores tumorales
Inicialmente, la expectativa de las investigaciones sobre los marcadores tumorales consistió en poder detectar en sus etapas iniciales todos los tipos de cáncer mediante un análisis de sangre, pero muy pocos poseen esta propiedad. Debido a estas razones, en la actualidad son principalmente usados en pacientes que ya hayan sido diagnosticados con cáncer para seguir su respuesta al tratamiento o para detectar recidivas. (9)
Durante el proceso de quimioterapia el nivel del marcador tumoral puede indicar cuándo hay necesidad de rediseñar la medicación si se comprueba el aumento mantenido del marcador. Es importante señalar que un aumento o disminución en los niveles de marcador observados en medidas seriadas se deben al cambio en la actividad tumoral y debe considerarse significativo cualquier alteración en los valores del intervalo de confianza para el 95 % respecto al valor previo; la especificidad de un marcador puede incrementarse ante la presencia de episodios benignos que pudieran alterar su valor.(9)
A continuación se expone una revisión de la evidencia científica de aspectos prácticos de los marcadores tumorales serológicos en el seguimiento de las principales neoplasias malignas.
Carcinomas Epiteliales de Ovarios
El cáncer de ovario es la cuarta causa de muerte por cáncer en mujeres con una supervivencia del 11 -20 %, en estadíos iniciales es silente y asintomático, y la mayoría se diagnostica en estadios avanzados de la enfermedad. El marcador tumoral de elección es el antígeno carbohidrato CA-125, aunque recientemente se ha incorporado la proteína epididimal humana 4 (HE4), un marcador tumoral que aumenta la sensibilidad en los estadios iniciales.(10)
Diagnóstico
El CA-125 se encuentra elevado en la mayoría (90%) de las mujeres con cáncer epitelial ovárico avanzado. Los niveles de CA-125 correlacionan bien con el volumen tumoral y estadio. Sin embargo, este marcador no tiene alta sensibilidad en la detección precoz (estadios I y II). Su especificidad es baja porque se puede elevar en algunos otros desórdenes ginecológicos (endometriosis, la miomatosis y la enfermedad pélvica inflamatoria). (11)
HE4 es un nuevo marcador, complementario al CA-125 en el diagnóstico de tumores de ovario. HE4 es una glicoproteína que se sobre expresa en el carcinoma epitelial de ovario pero no en condiciones benignas. Utilizado como marcador único posee mayor sensibilidad y especificidad que el CA-125, pero la mayor utilidad radica en la medición simultánea de ambos antígenos CA-125+HE4, ya que la sensibilidad y especificidad al momento del diagnóstico es superior cuando se los compara con cada uno de ellos por separado. (11)
La FDA (Food and Drug Administration) autorizó el uso de CA-125+HE4 con el algoritmo del riesgo de malignidad ovárica (ROMA) para estimar el riesgo de cáncer de ovario en mujeres con una masa pélvica, ya que mejora significativamente la capacidad para identificar a las mujeres pre y post menopáusicas que se encuentran en alta o baja probabilidad de cáncer de ovario cuando se presentan con un quiste ovárico o masa. (11)
Pronóstico y seguimiento
La determinación del ROMA permite que a la hora de la cirugía se tomen cuidados diferentes, se realiza una evaluación exhaustiva de todo el contenido del peritoneo pélvico y abdominal, lavados, histerectomía abdominal total, múltiples biopsias del peritoneo para ver si existen metástasis y evaluación de los ganglios linfáticos. Los pacientes sometidos a estos cuidados específicos antes y durante la cirugía aumentan las tasas de supervivencia. (12)
Otra utilidad del índice ROMA radica en que mejora el seguimiento de los pacientes, ya que HE4 aumenta en las recurrencias pero permanece disminuido en el 75% de los que no tienen progresión. Por lo tanto la medición simultánea previa a los ciclos de tratamiento es útil para conocer el estado y la respuesta del paciente. Ayuda a determinar de manera más temprana la recurrencia del tumor. (12)
Cáncer de Próstata
El cáncer de próstata es el tumor maligno con mayor prevalencia en el mundo occidental, se presenta en aproximadamente el 30% de los varones con edad superior a los 50 años. El marcador tumoral de elección es el antígeno específico de próstata (PSA). Actualmente las guías recomiendan herramientas con mayor especificidad que el PSA, por ejemplo el cociente PSA total/PSA libre. (13)
El porcentaje de PSA libre varía en función de la patología prostática, siendo más bajo en pacientes con cáncer de próstata. La mayoría de los estudios recomiendan la realización del cociente en pacientes con valores de PSA total comprendido entre 4-10 ng/ml y aunque se han propuesto varios puntos de corte del cociente PSA total/PSA libre para aumentar la especificidad, la mayoría de los estudios emplean un cociente inferior a 20 como sospecha de neoplasia.(13)
Diagnóstico precoz
Los estudios realizados sobre el diagnóstico precoz del cáncer de próstata no han demostrado una disminución de la mortalidad por este tumor, por ello no está indicada su realización de
forma generalizada en la población de posible riesgo. (3) No obstante, algunas sociedades
científicas como la American Cancer Society y la American Urological Association recomienda la determinación anual de PSA y tacto rectal a partir de los 50 años. (13)
Un aumento del PSA en ausencia de neoplasia se debe mayormente a procesos benignos como la prostatitis y adenoma prostático. (13)
Pronóstico y Seguimiento
Diversos autores han indicado que niveles de PSA bajos antes de la cirugía están relacionados con una mayor tasa de supervivencia. (13) Así también se ha considerado la velocidad de PSA como una herramienta útil en el pronóstico de la enfermedad, así incrementos de PSA mayores de 2 ng/ml /año está asociado con una menor supervivencia. (14)
Como la mayoría de los marcadores tumorales, el PSA es muy útil para el diagnóstico precoz de recidivas y se recomienda su determinación seriada, de manera que dos aumentos sucesivos de PSA serían indicativos de recidiva.
Cáncer de Mama
El cáncer de mama es el de mayor prevalencia en la mujer y una de las principales causas de muerte en ellas. Su incidencia se incrementa con la edad. Los marcadores tumorales de elección en el cáncer de mama son el antígeno carbohidrato CA15.3 y el antígeno carcinoembrionario (CEA). En algunos subgrupos de pacientes con cáncer de mama con sobreexpresión de la oncoproteína HER2-Neu, puede ser de gran utilidad la determinación sérica del mismo. (15)
Diagnóstico
Únicamente un 10% de los tumores de este tipo, en estadios iniciales presentan niveles elevados de CA15.3, mientras que este porcentaje se incrementa hasta un 70% en estadios avanzados de la enfermedad, por lo tanto, este marcador tumoral no es útil para el diagnóstico precoz, pero sí puede ser un apoyo para el diagnóstico junto con otras exploraciones complementarias. (16)
Aunque el CEA es menos sensible que el CA15.3, se recomienda su inclusión para alcanzar mayor sensibilidad, ya que existe un pequeño porcentaje de tumores (10%) que son CA15.3 negativos y CEA positivos.(16)
Pronóstico y Seguimiento
La mayoría de los estudios publicados coinciden en la utilidad del CEA y CA15.3 como factor pronóstico en el cáncer de mama, siendo el valor del CEA superior al del CA15.3. A mayores valores de marcadores tumorales preoperatorios mayor probabilidad de recidiva, así la mayoría de las pacientes con una concentración de CEA superior a 7,5 ng/ml preoperatorio presentaran recidiva tumoral. (17)
Los niveles de CA 15.3 se relacionan con el curso de la enfermedad durante el tratamiento en el 60 % de los pacientes con enfermedad metastásica frente a un 40 % para el CEA. Esto puede ser muy importante a la hora de mantener o cambiar un tratamiento concreto, de ahí la importancia de la monitorización de los marcadores durante el tratamiento de una neoplasia invasora conocida. (17)
En el caso del HER2-Neu, aunque el número de estudios publicados es menor, también ha mostrado utilidad en la detección de recidivas en pacientes con sobreexpresión tisular. La determinación seriada conjunta de CEA y CA15.3 es de gran utilidad en la detección precoz de recidivas, pudiendo aparecer incrementos hasta 18 meses antes del diagnóstico de recidivas, algunos estudios demuestran que puede ser el primer marcador de recidiva en tumores con sobreexpresión. (17)
Se aconseja la utilización del incremento dinámico, la determinación seriada de donde dos incrementos sucesivos de un 15% respecto al resultado anterior serían indicativos de recidiva con una especificidad del 99%.(17)
Cáncer de Colon
El cáncer de colon afecta aproximadamente a uno de cada 20 individuos y en especial a la población anciana. El marcador tumoral de elección es el CEA, aunque se recomienda la utilización de otros marcadores tumorales como el antígeno carbohidrato CA19.9, aunque su aportación es mínima. (18)
Diagnóstico
Como ocurre con la mayoría de los marcadores tumorales, la sensibilidad del CEA en el cáncer de colon va unida al tiempo de evolución, alcanzando una sensibilidad de 65-90% en estadios avanzados, por lo que no se aconseja su uso en el diagnóstico precoz.(19)
Pronóstico y Seguimiento
Se considera que el CEA puede ser de utilidad como indicador pronóstico en combinación con otros factores. Los estudios respecto a la utilidad del CA19.9 como factor pronóstico no son concluyentes Diversos estudios han demostrado que el CEA es el primer signo de recidiva, por lo que las guías clínicas recomiendan su determinación sérica cada dos o tres meses. (20)
No obstante, no se debe olvidar que hay recidivas con marcadores tumorales negativos, por lo que ante una sospecha clínica de recidiva y ausencia de marcadores tumorales deben realizarse otras pruebas complementarias, esto es específico para todos los tipos de cáncer.
La incorporación del CA19.9 en el diagnóstico precoz de recidiva sólo mejora la sensibilidad en el 5% de los casos. (20)
Respecto a su valor pronóstico, múltiples estudios han demostrado que cuanto mayor es la concentración del CEA preoperatorio, más probabilidad hay de una recidiva postoperatoria y en un período más breve.(18) La concentración de CEA posterior a una resección completa del tumor debe normalizarse entre 1 y 4 meses después de la intervención. Una elevación postquirúrgica persistente indica resección incompleta o recurrencia. (20)
Otros marcadores tumorales estudiados en el cáncer de colon han sido los antígenos carbohidratos CA 242, CA 72.4 (TAG-72) y CA 50; los antígenos polipeptídicos tisular (TPA) y tisular específico (TPS), así como el inhibidor tisular de metaloproteinasa 1 (TIMP-1). (19)
Los resultados obtenidos en los diferentes estudios concluyen que todos estos marcadores pueden complementar al CEA en el momento del diagnóstico y ofrecer información pronostica, pero no se recomienda su uso en el seguimiento, ya que ninguno de ellos ha demostrado ser más sensible que el CEA en la detección de recurrencias. (19)
Cáncer de Pulmón
El cáncer de pulmón es el más frecuente del mundo, con aproximadamente 1.400.000 nuevos casos al año. Los tipos histológicos tienen diferente evolución natural y, por tanto, como paso previo al tratamiento, es necesario un diagnóstico histológico preciso. (21)
Las principales decisiones con respecto al tratamiento se realizan al distinguir claramente los carcinomas indiferenciados de célula pequeña (CICP) y los que no corresponden a este tipo (NCICP), subclasificados a su vez en diferentes tipos histológicos (principalmente adenocarcinoma, escamoso y carcinoma indiferenciado de células grandes).(21)
Los marcadores tumorales de elección en el caso de los NCICP son el CEA, la citoqueratina CYFRA 21 -1 y el antígeno asociado a los carcinomas escamosos (SCC), en algunas ocasiones se puede utilizar el CA-125, CA19.9 y CA15.3, siendo el CYFRA 21 -1 el que predomina en los carcinomas escamosos junto con el SCC, que presenta la mayor especificidad para este tipo histológico. (21)
El CEA es el que presenta mayores concentraciones en los adenocarcinomas, pero su especificidad es relativa porque también puede aparecer en CICP. Los marcadores tumorales de elección en el caso de los CICP son la enolasa neuroespecífica (NSE), el péptido asociado a la progastrina (ProGRP) y la cromogranina A, siendo el pro GRP el que tiene mayor sensibilidad y especificidad en tumores CICP intratorácicos. (21)
De acuerdo con resultados previos, incrementos de ProGRP >150 pg/ml indican con una alta probabilidad (>98%) de CICP o tumor neuroendocrino. (21)
El SCC predomina en los NCICP, principalmente escamosos. Otros marcadores tumorales, como el CEA, el CA 15.3 y el CYFRA 21-1, predominan en los NCICP, en los adenocarcinomas los dos primeros, y en los escamosos el último. Utilizando estos seis marcadores tumorales ante la sospecha de neoplasia pulmonar se puede sugerir el diagnóstico histológico en el 80% de los casos, con una correlación con la histología del 90%. (21)
Los marcadores tumorales muestran una clara relación con el estadio tumoral, con niveles significativamente superiores en pacientes con neoplasias avanzadas. (21)
Diagnóstico
La utilidad de los marcadores tumorales en el cáncer de pulmón es controvertida y prácticamente ninguna guía clínica la aconseja, aunque en ocasiones el análisis de los marcadores tumorales ante una sospecha clínica puede ayudar al diagnóstico. (22)
Pronóstico y Seguimiento
La mayoría de los estudios consideran que la determinación pretratamiento de los marcadores tumorales en el cáncer de pulmón tiene valor pronóstico. En el caso del NCICP todos los marcadores tumorales han mostrado utilidad; SCC, CEA, CA125 y CYFRA21 -1. En el caso del CICP la mayoría de los estudios se han realizado con la NSE, al ser el ProGRP un marcador tumoral de reciente incorporación al panel de los marcadores tumorales en cáncer de pulmón. (22)
Hay pocos estudios que evalúen la utilidad de los marcadores tumorales en el seguimiento y la detección de recidivas al tratarse de un tipo de tumor altamente agresivo y con una baja tasa de supervivencia, por lo cual la aplicación de los marcadores tumorales para la detección de recidivas no está incluida en las guías clínicas.(22)
Cáncer Hepático
El cáncer de hígado según la OMS ocupa el segundo lugar después del cáncer de pulmón, estimándose que cada año se diagnostican más de 250.000 casos. La enfermedad es especialmente frecuente en los países del sudeste de Asia, donde se estima que ocasiona 150 fallecimientos por 100.000 habitantes por año. (23)
Diagnóstico precoz
No existen recomendaciones internacionales para el diagnóstico precoz de esta enfermedad, aunque la mayoría de las sociedades científicas recomienda la utilización del cribado en pacientes de alto riesgo (cirrosis hepática secundaria a VHB o VHC, hepatitis alcohólica, hemocromatosis, hepatitis autoinmune y pacientes con antecedentes familiares de cáncer de hígado), junto con la ecografía hepática. (24)
Aunque el diagnóstico final de cáncer de hígado se hace por biopsia, en el caso de encontrarse valores de AFP > 200ng/ml en pacientes con una masa >2cm, se podría evitar la biopsia. Algunos autores cuestionan su empleo por el elevado número de falsos positivos, porque se pueden encontrar valores elevados de AFP en hepatopatías, aunque esta suele encontrarse a bajas concentraciones. (24)
Pronóstico y Seguimiento
El aumento de AFP podría ayudar a identificar subgrupos de pacientes con un mayor riesgo de recidiva precoz y mal pronóstico después de la hepatectomía. La positividad de AFP es un factor de riesgo independiente de recidiva y mortalidad, siendo peor el pronóstico en aquellos pacientes con AFP> 400ng/ml y en aquellos pacientes con persistencia de AFP en suero tras la resección quirúrgica indicando la persistencia de algún resto tumoral. (24)
Uno de los problemas en el diagnóstico diferencial del hepatocarcinoma y la hepatitis o cirrosis es que la AFP puede estar elevada, concentraciones superiores al valor discriminante de 9 U/ml en estas condiciones benignas. (24)
Para descartar estos falsos positivos se dispone de diferentes aproximaciones, como separar las isoformas de AFP específicas de patología tumoral o benigna mediante lecitinas, que se unen a diferentes residuos glucosilados, o valorar incrementos significativos en las concentraciones de AFP en patología benigna la concentración de AFP se mantiene estable o disminuye.(24)
Cáncer de Páncreas
Se estima que cada año se diagnostican unos 233.000 nuevos casos en todo el mundo. Las formas más habituales de cáncer de páncreas exocrino son los adenocarcinomas (más del 95%). El marcador tumoral de elección es el CA19.9. (25)
Diagnóstico
La concentración de CA19.9 es baja en estadios iniciales, con lo cual no es útil para el diagnóstico precoz, pero sí que ayuda al diagnóstico, ya que la mayoría de los pacientes tienen valores elevados en el momento del diagnóstico, y en ocasiones la sintomatología es similar a la que aparece en otras neoplasias digestivas o incluso en procesos no tumorales, como las enfermedades inflamatorias pancreáticas. (26)
Hay que considerar la presencia de niveles elevados de CA19.9 en patologías benignas como en hepatopatías con ictericia y en pancreatitis (en ocasiones hasta 1000 U/ml). (26)
Dentro de los marcadores moleculares estudiados en el cáncer de páncreas, el oncogen K-ras es el que ofrece mejores resultados debido a la alta frecuencia de mutaciones descritas en el codón 12 (65-100%, dependiendo de la sensibilidad del método y el área geográfica evaluada) y a que es un episodio precoz en la carcinogénesis pancreática. Estudios recientes han demostrado su capacidad para el diagnóstico del cáncer de páncreas, pero no se ha evaluado su empleo en el pronóstico y seguimiento de esta enfermedad. (26)
Pronóstico y Seguimiento
El CA19.9 también ha mostrado gran utilidad como factor pronóstico, así valores preoperatorios por encima de >1000 U/ml y el mantenimiento de niveles elevados de CA19.9 tras la cirugía serán indicativos de un mal pronóstico. (27)
Al tratarse un tumor agresivo y con una elevada tasa de mortalidad, existen pocos estudios sobre la utilidad del CA19.9 en la detección precoz de recidivas, aunque si es útil las determinaciones seriadas de CA19.9 para valorar la respuesta al tratamiento. Durante la terapia definitiva y después de ella, el aumento de la concentración de CA 19.9 puede identificar a los pacientes con crecimiento evolutivo del tumor. Sin embargo, la presencia de una concentración normal de CA 19-9 no evita la recidiva. (27)
Conclusiones
Los marcadores tumorales son en muy pocas ocasiones empleados para el diagnóstico y no pueden reemplazar a la biopsia para detectar el cáncer. Una elevación de un marcador no indica necesariamente la presencia de una neoplasia. Los resultados dentro de límites normales no excluyen malignidad o progresión.
Referencias bibliográficas
1. Reiter M, Costello J, Schwope R, Lisanti C, Osswald M. Review of commonly used serum tumor markers and their relevance for image interpretation. J Compot Assist Tomogr. 2015 [citado 18/01/2020]; 39(6): 825-834. Disponible en: https://journals.lww.com/jcat/FullText/2015/11000/Review_of_Commonly_Used_Serum_Tumor_Markers_and.1.aspx
2. Serrano J. Los marcadores biológicos de cáncer. Natura Medicatrix. 2001 [citado 18/01/2020]; 19(6):272-278. Disponible en: https://dialnet.unirioja.es/servlet/articulo?codigo=4989310
3. Bast RC, Ravdin P, Hayes DF, Bates S, Fritsche H, Jessup JM, ET AL. 2000 Update of recommendations for the use of tumors markers in breast and colorectal cancer: clinical practice guidelines, of the American Society of Clinical Oncology. J Clin Oncol. 2001[citado 18/01/2020]; 19(6): 4185-4188. Disponible en: https://ascopubs.org/doi/full/10.1200/JCO.2001.19.6.1865
4. Litviakov NV, Bychkov VA, Stakheeva MN, Ibragimova MK, Tsyganov MM, Gaptulbarova KA. Breast tumor cell subpopulations with expression of the OCT4 proteins. J Mol Hist.2020 [citado 18/01/2020];51(6):717-728. Disponible en: https://link.springer.com/article/10.1007/s10735-020-09917-1
5. Cuba. Ministerio de Salud Pública. Anuario estadístico de Cuba. La Habana: MINSAP; 2018
6. Hermida Lazcano I, Sánchez Tejero E, Nerín Sánchez C, Cordero Bernabé R, Mora Escudero I, Pinar Sánchez J. Marcadores Tumorales. Rev Clin Med Fam. 2016 [citado 06/01/2020]; 9(1):31-42. Disponible en: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1699-695X2016000100006
7. Lavín de Juan L. Marcadores Tumorales: Presente y Futuro. [Tesis]. [España]: Universidad Complutense; 2015. 22 p. Disponible en: https://eprints.ucm.es/id/eprint/48763/1/LAURA%20LAVIN%20DE%20JUAN%20(1).pdf
8. Kasper LD, Fauc AS, Hauser LS, Longo LD, Jameson JL, Loscalzo J. Harrison: Principios de Medicina Interna.19na ed. México, D.F: Mcgraw-Hill Interamerican. 2015 [citado 18/01/2020]. Disponible en: https://www.academia.edu/40121481/P_R_I_N_C_I_P_I_O_S_H_A_R_R_I_S_O_N_H_A_R_R_I_S_O_N
9. Noya Chaveco ME, Moya González NL, Llamos Sierra N, Morales Larramendi R, Cardona Garbey DL, Filiú Ferrera JL, Del Valle Díaz S, et al. Roca Goderich: Temas de Medicina interna. 5ta ed. La Habana: Ciencias Médicas; 2017.
10. Tahmasebi F, Nath R, Sokolovsky N, Scaoli J, Boley J, Mehra G, et al. Incidental Finding of Raised CA125: a Cause for Concern. Crit Care Obst Gyne. 2018 [citado 15/01/2020];5(1):3. Disponible en: https://obstetrics.imedpub.com/incidental-finding-of-raised-ca125-a-cause-for-concern.php?aid=23936
11. Chen F, Shen J, Wang J, Cai P, Huang Y. Clinical analysis of four serum tumors markers in 458 patients with ovarian tumors: diasnostic value of the combined use of HE4, CA125, CA19-9 and CEA in ovarian tumors. Cancer Manag Res.2018[citado 18/01/2020]; 10: 1313-1318. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5968799/
12. Nowak M, Janas L, Stachowiak G, Stetkiewicz T, Wilczynski JR. Current clinical aplication of serum biomarkers to detect ovarian cancer. Prz Menopauzalny. 2015 [citado 18/01/2020]; 14(4):254-259. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4733894/
13. Vitkin N, Nersesian S, Siemens RD, Koti M. The tumor inmune contexture of prostate cancer. Front Inmunol. 2019 [citado 27/01/2020]; 10:603. Disponible en: https://www.frontiersin.org/articles/10.3389/fimmu.2019.00603/full
14. López Ríos L, Sánchez Montero IR, García Moreno I. Relación entre el marcador tumoral antígeno prostático específico y la mortalidad por cáncer de próstata. CCM. 2017 [citado 18/01/2020]; 21(1): 100-111. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1560-43812017000100009
15. Salman JW, Schoots IG, Carlsson SV, Jenster G, Roobol MJ .Prostate Specific Antigen as a tumor marker in prostate cancer: biochemical and clinical aspects. Adv Exp Med Biol. 2015[citado 18/01/2020]; 867: 93-114. Disponible en: https://link.springer.com/chapter/10.1007/978-94-017-7215-0_7
16. Davis AA, Pierga JY, Dirix LY, Stefan Michiels S, Alfred Rademaker A, Reuben JM, et al. The impact of circulating tumor cells (CTCs) detection in metastatic breast cancer (MBC): Implications of “indolent” stage IV disease (Stage IV indolent). J Clin Oncol. 2018[citado 18/01/2020];36(15 Suppl):1019. Disponible en: https://ascopubs.org/doi/10.1200/JCO.2018.36.15_suppl.1019
17. Reyes García N, Miranda Devora G. Marcadores tumorales en el cáncer de mama: CA 15-3 y antígeno carcinoembrionario. Rev Mex Mastol.2016 [citado 16/01/2020]; 6(1):9-13. Disponible en: https://www.medigraphic.com/pdfs/revmexmastol/ma-2016/ma161c.pdf
18. Roa I, Sánchez T, Majlis A, Schalper K. Mutación del gen K-RAS en el cáncer de colon y recto. Rev Med Chile. 2013[citado 16/01/2020]; 141(9):1166-1172. Disponible en: https://scielo.conicyt.cl/scielo.php?script=sci_arttext&pid=S0034-98872013000900009
19. OncoLink Team. Tumor Markers for Colorectal Cancer. Philadelphia: University of Pennsylvania [08/09/2020; citado 28/09/2020]. Disponible en: https://www.oncolink.org/cancers/gastrointestinal/colon-cancer/treatments/tumor-markers-for-colorectal-cancer
20. Takahashi R, Sakamoto K, Sugimoto K, Motegi S, Tsukamoto R, Ichikawa R, et al. Significance of serum p53 antibody as a tumor marker in colorectal cancer. Dis Markers.2019 [citado 18/01/2020]; 2019: 2721876. Disponible en: https://www.hindawi.com/journals/dm/2019/2721876/
21. Cuba. Centro Nacional de Información de Ciencias Médicas. Biblioteca MédicaNacional. Cáncer de pulmón, tráquea y bronquios. Tratamiento y Factores de riesgo. Bibliomed. 2019[citado 25/08/2019];26(3). Disponible en: http://files.sld.cu/bmn/files/2019/03/bibliomed-marzo-2019.pdf
22. Wadowska K , Bil Lula I, Trembecki L, Sliwinska Mosson M. Genetic markers in lung cancer diagnosis: A review. Int J Mol Sci.2020[citado 18/01/2020];21(13):4569. Disponible en: https://www.mdpi.com/1422-0067/21/13/4569
23. Mora Morales E, Denis Rodríguez PB, Melo SG, Aguirre GAA. Utilidad de la inmunohistoquímica en el diagnóstico del hepatocolangiocarcinoma. Rex Mex Forense. 2018[citado 18/01/2020];3(2):47-53. Disponible en: https://www.medigraphic.com/cgi-bin/new/resumen.cgi?IDARTICULO=88021
24. Ibrahim Alhadi M, Kumar Chutturghoon V, Kwabena G, Zhu H, Yang Zhen T, Yang Xie H, et al. Serum Biomarkers AFP, CEA and CA19-9 combined detection for early diagnosis of hepatocellular carcinoma. Iran J Public Health. 2019[citado 18/01/2020]; 48(2):314–322. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6556181/
25. Gzil A, Zarębska I, Bursiewicz W, Antosik P, Grzanka D, Szylberg L. Markers of pancreatic cancer stem cells and their clinical and therapeutic implications. Mol Biol Repo. 2019[citado 18/01/2020];46(6):6629–6645. Disponible en: https://link.springer.com/article/10.1007/s11033-019-05058-1
26. Seufferlein T, Ettich T. Treatment of pancreatic cancer- neoadjuvant treatment in resectable pancreatic cancer (PDCA). Trasl Gastroenterol Hepatol.2019[citado 18/01/2020]; 4:21. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6458347/
27. Jose Lahoud M, Kourie Raphael H, Antoun J, El Osta L, Ghosn M. Road map for pain management in pancreatic cancer: A review. World J Gastointest Oncol.2016 [citado 06/01/2020]; 8(8): 599-606. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4980650/
Declaración de conflicto de intereses
Los autores declaran no tener conflictos de intereses.
Declaración de fuentes de financiación
No se recibió financiación para el desarrollo de la presente investigación.
Publicación cuatrimestral de la
Universidad de Ciencias Médicas de Holguín ![]() CC-BY-NC 4.0
CC-BY-NC 4.0